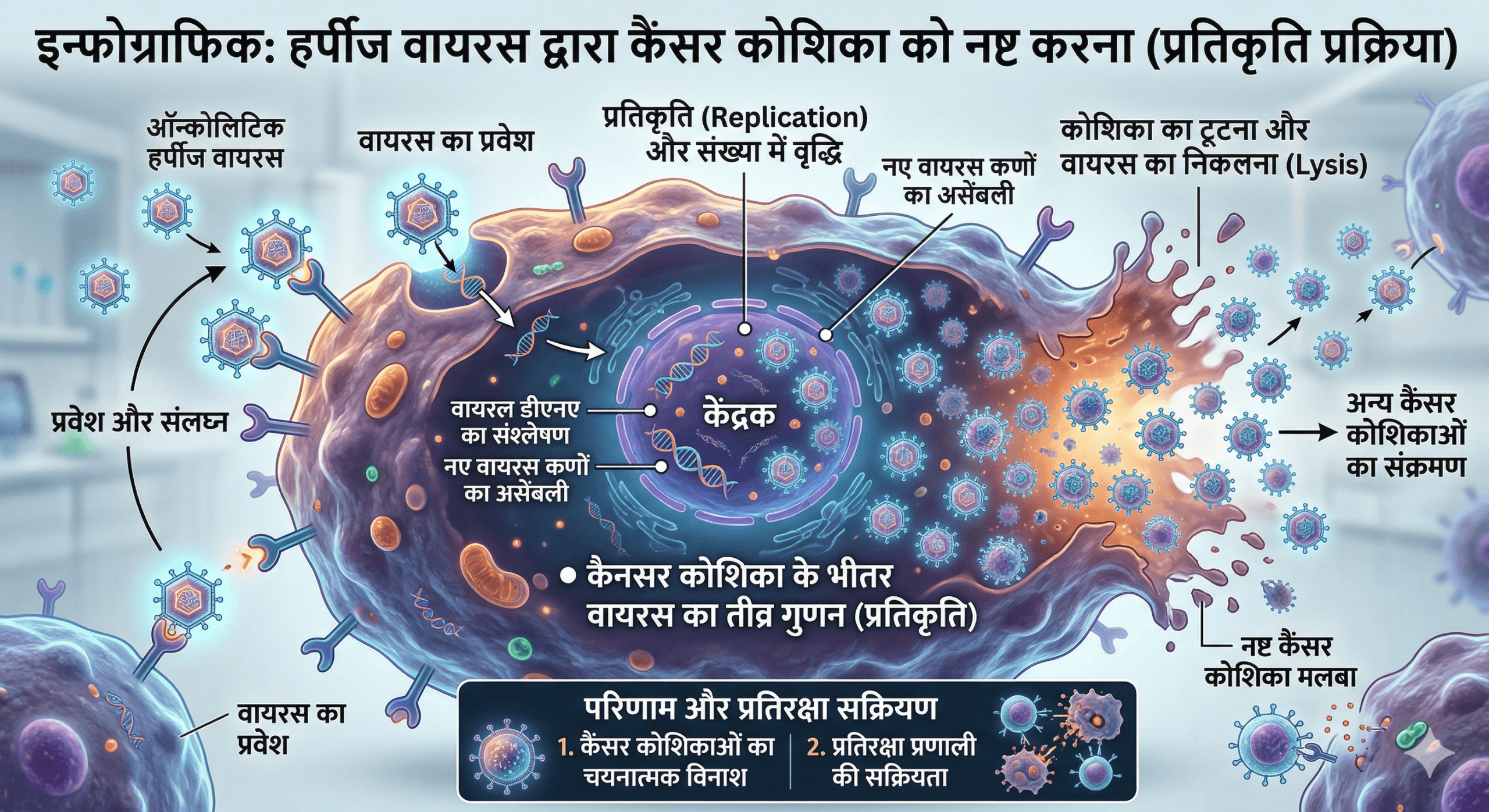
चिकित्सा जगत के इतिहास में कुछ खोजें ऐसी होती हैं जो हमारी सोच की दिशा को पूरी तरह बदल देती हैं। कैंसर के इलाज में हर्पीज वायरस का उपयोग (Oncolytic Herpes Virus Therapy) एक ऐसी ही क्रांतिकारी खोज है जिसने एक घातक दुश्मन को एक रक्षक के रूप में स्थापित कर दिया है। जिस हर्पीज सिम्प्लेक्स वायरस (HSV-1) को हम दशकों से केवल कष्टदायक ‘कोल्ड सोर’ या छालों का कारण मानते थे, आज वही वायरस आनुवंशिक रूप से संशोधित होकर कैंसर की जटिल कोशिकाओं को भीतर से नष्ट करने का सबसे शक्तिशाली हथियार बन चुका है । इस तकनीक को ‘ऑन्कोलिटिक विरोथेरेपी’ कहा जाता है, जहाँ वायरस को इस तरह से ‘प्रोग्राम’ किया जाता है कि वह स्वस्थ कोशिकाओं को नुकसान पहुँचाए बिना केवल कैंसर कोशिकाओं को ही लक्षित करे। आधुनिक विज्ञान ने यह सिद्ध कर दिया है कि कैंसर के इलाज में हर्पीज वायरस का उपयोग न केवल ट्यूमर को सीधे नष्ट करने में सक्षम है, बल्कि यह शरीर की सुप्त प्रतिरक्षा प्रणाली (Immune System) को भी सक्रिय करता है, जिससे वह भविष्य में होने वाले पुनरावृत्ति के खतरों से लड़ने के लिए तैयार हो सके ।
विरोथेरेपी का उदय: एक ऐतिहासिक विडंबना से आधुनिक समाधान तक
कैंसर के इलाज के लिए वायरस के उपयोग की अवधारणा सुनने में जितनी आधुनिक लगती है, इसकी जड़ें उतनी ही पुरानी हैं। बीसवीं सदी की शुरुआत में वैज्ञानिकों ने पहली बार देखा कि कुछ रोगियों में वायरल संक्रमण के बाद उनके कैंसर ट्यूमर में अप्रत्याशित कमी आई। 1904 की एक प्रसिद्ध घटना में, गर्भाशय ग्रीवा के कैंसर से पीड़ित एक महिला को एक पागल कुत्ते ने काट लिया था। रेबीज के टीके (जो वायरस का एक कमजोर रूप था) के प्रशासन के बाद, उसका विशाल ट्यूमर गायब हो गया और वह अगले आठ वर्षों तक पूरी तरह स्वस्थ रही । यह प्रारंभिक अवलोकन विरोथेरेपी की नींव बना।
हालांकि, उस समय की तकनीक इतनी उन्नत नहीं थी कि वायरस की घातक प्रकृति को नियंत्रित किया जा सके। शुरुआती परीक्षणों में, प्राकृतिक (Wild-type) वायरस अक्सर रोगी के अंगों को ही संक्रमित कर देते थे, जिससे लाभ के बजाय हानि अधिक होती थी। 1990 के दशक में आनुवंशिक इंजीनियरिंग (Genetic Engineering) के विकास के साथ ही कैंसर के इलाज में हर्पीज वायरस का उपयोग संभव हो पाया । वैज्ञानिकों ने सीखा कि कैसे वायरस के उस हिस्से को काट दिया जाए जो बीमारी फैलाता है और उसके स्थान पर ऐसे जीन डाल दिए जाएं जो केवल कैंसर कोशिकाओं को पहचान सकें। आज, विरोथेरेपी न केवल एक प्रयोग है, बल्कि FDA द्वारा स्वीकृत एक उपचार पद्धति है जिसने हजारों रोगियों के जीवन को नई दिशा दी है ।
कैंसर के इलाज में हर्पीज वायरस का उपयोग: वैज्ञानिक कार्यप्रणाली
हर्पीज सिम्प्लेक्स वायरस टाइप 1 (HSV-1) को ऑन्कोलिटिक विरोथेरेपी के लिए सबसे पसंदीदा उम्मीदवार माना जाता है। इसके कई वैज्ञानिक कारण हैं। सबसे पहले, HSV-1 का जीनोम (Genome) बहुत बड़ा और स्थिर होता है, जिसमें लगभग 152 kb डीएनए होता है। इसका मतलब है कि वैज्ञानिक इसमें कई बाहरी जीन (Transgenes) आसानी से जोड़ सकते हैं जो उपचार की प्रभावशीलता को बढ़ाते हैं । दूसरा, इस वायरस की प्रकृति बहुत अधिक ‘लाइटिक’ (Lytic) होती है, जिसका अर्थ है कि यह कोशिका के भीतर प्रवेश करने के बाद उसे बहुत तेजी से नष्ट करने की क्षमता रखता है।
वैज्ञानिक दृष्टि से, कैंसर कोशिकाएं और स्वस्थ कोशिकाएं वायरस के प्रति अलग-अलग प्रतिक्रिया करती हैं। स्वस्थ कोशिकाओं में एक पूर्ण एंटी-वायरल रक्षा प्रणाली होती है जिसे ‘टाइप I इंटरफेरॉन पाथवे’ कहा जाता है। जब कोई वायरस स्वस्थ कोशिका पर हमला करता है, तो यह पाथवे सक्रिय हो जाता है और वायरस की प्रतिकृति को रोक देता है। इसके विपरीत, कैंसर कोशिकाएं अपनी वृद्धि को अनियंत्रित रखने के लिए अक्सर इन रक्षा प्रणालियों को बंद कर देती हैं। कैंसर के इलाज में हर्पीज वायरस का उपयोग इसी जैविक छिद्र (Biological loophole) का फायदा उठाता है । चूंकि संशोधित वायरस केवल उन कोशिकाओं में अपनी संख्या बढ़ा सकता है जहाँ रक्षा तंत्र कमजोर है, इसलिए यह स्वस्थ कोशिकाओं को छोड़ देता है और केवल कैंसर कोशिकाओं का शिकार करता है ।
| वायरस का घटक | कैंसर कोशिका में व्यवहार | स्वस्थ कोशिका में व्यवहार |
| प्रवेश (Entry) | नक्टिन-1 (Nectin-1) रिसेप्टर्स के माध्यम से त्वरित प्रवेश । | सीमित प्रवेश या प्रवेश के बाद निष्क्रियता। |
| प्रतिकृति (Replication) | अवरुद्ध एंटी-वायरल पाथवे के कारण तीव्र प्रतिकृति । | इंटरफेरॉन पाथवे द्वारा प्रतिकृति का पूर्ण दमन। |
| विनाश (Lysis) | कोशिका का फटना और नए वायरस का निकलना । | कोशिका सुरक्षित रहती है। |
आनुवंशिक इंजीनियरिंग: वायरस को ‘स्मार्ट किलर’ बनाने की कला
कैंसर के इलाज में हर्पीज वायरस का उपयोग करने के लिए इसे ‘जेनेटिकली मॉडिफाई’ करना एक अत्यंत जटिल प्रक्रिया है। वैज्ञानिकों का मुख्य उद्देश्य वायरस को सुरक्षित बनाना और इसकी मारक क्षमता को बढ़ाना होता है। इसके लिए मुख्य रूप से तीन प्रकार के आनुवंशिक परिवर्तन किए जाते हैं जो इसे एक सामान्य रोगजनक से एक जीवन रक्षक दवा में बदल देते हैं।
प्रथम चरण में, वायरस के उस जीन को हटा दिया जाता है जिसे ‘ICP34.5’ कहा जाता है। यह जीन वायरस को नसों की कोशिकाओं (Neurons) को संक्रमित करने में मदद करता है। इस जीन के हटने से वायरस स्वस्थ तंत्रिका कोशिकाओं को नुकसान नहीं पहुँचा पाता, जिससे हर्पीज का सामान्य संक्रमण होने का खतरा समाप्त हो जाता है । द्वितीय चरण में, ‘ICP47’ नामक जीन को हटाया जाता है। यह जीन सामान्यतः वायरस को शरीर की प्रतिरक्षा प्रणाली से छिपाने का काम करता है। जब इसे हटा दिया जाता है, तो संक्रमित कैंसर कोशिकाएं प्रतिरक्षा प्रणाली के लिए ‘दृश्य’ हो जाती हैं, जिससे शरीर की अपनी कोशिकाएं भी ट्यूमर पर हमला करना शुरू कर देती हैं ।
तृतीय और सबसे महत्वपूर्ण चरण में, वायरस के डीएनए में एक मानवीय जीन जोड़ा जाता है जिसे ‘GM-CSF’ (Granulocyte-Macrophage Colony-Stimulating Factor) कहते हैं। यह जीन एक विशेष प्रोटीन बनाता है जो शरीर की श्वेत रक्त कोशिकाओं, विशेष रूप से डेंड्रिटिक कोशिकाओं (Dendritic Cells) को ट्यूमर की ओर आकर्षित करता है । यह प्रक्रिया विरोथेरेपी को न केवल एक स्थानीय उपचार बनाती है, बल्कि इसे एक ‘सक्रिय वैक्सीन’ में बदल देती है जो पूरे शरीर में फैले कैंसर के खिलाफ काम करती है ।
T-VEC (Imlygic): विरोथेरेपी के क्षेत्र में पहली वैश्विक सफलता
विरोथेरेपी के आधुनिक युग की शुरुआत 2015 में हुई जब Talimogene Laherparepvec (T-VEC), जिसे ‘Imlygic’ ब्रांड नाम से जाना जाता है, को FDA की मंजूरी मिली । यह कैंसर के इलाज में हर्पीज वायरस का उपयोग करने वाली दुनिया की पहली स्वीकृत दवा बनी। इसका मुख्य उपयोग उन्नत मेलेनोमा (Melanoma) के इलाज के लिए किया जाता है, जो त्वचा का सबसे घातक कैंसर है और जो सर्जरी के माध्यम से पूरी तरह से हटाया नहीं जा सकता।
T-VEC की सफलता ने यह प्रमाणित किया कि वायरस को एक दवा के रूप में सुरक्षित रूप से इंजेक्ट किया जा सकता है। इसे सीधे ट्यूमर के अंदर सुई के माध्यम से दिया जाता है। नैदानिक परीक्षणों (OpTIM Phase III Trial) में देखा गया कि जिन रोगियों को T-VEC दिया गया, उनमें ‘ड्यूरेबल रिस्पांस रेट’ (Durable Response Rate) उन रोगियों की तुलना में काफी अधिक था जिन्हें पारंपरिक उपचार दिया गया था ।
T-VEC उपचार की समय-सारणी और खुराक
| उपचार का चरण | समय सीमा | उद्देश्य |
| प्रारंभिक खुराक (Dose 1) | दिन 1 | वायरस को ट्यूमर के वातावरण से परिचित कराना । |
| द्वितीय खुराक (Dose 2) | 3 सप्ताह बाद | प्रतिरक्षा प्रतिक्रिया को सक्रिय करना । |
| अनुवर्ती खुराक (Subsequent Doses) | प्रत्येक 2 सप्ताह में | ट्यूमर कोशिकाओं का निरंतर विनाश । |
| उपचार की अवधि | 6 महीने या उससे अधिक | जब तक इंजेक्ट करने योग्य ट्यूमर शेष न रहें । |
T-VEC के प्रयोग के दौरान वैज्ञानिकों ने एक अद्भुत घटना देखी जिसे ‘एब्सकोपल इफेक्ट’ (Abscopal Effect) कहा जाता है। इसमें देखा गया कि जब एक ट्यूमर में वायरस इंजेक्ट किया गया, तो शरीर के दूसरे हिस्सों में मौजूद अन-इंजेक्टेड ट्यूमर भी सिकुड़ने लगे । यह इस बात का प्रमाण था कि कैंसर के इलाज में हर्पीज वायरस का उपयोग केवल स्थानीय स्तर पर काम नहीं करता, बल्कि यह पूरे शरीर की प्रतिरक्षा प्रणाली को कैंसर के विरुद्ध ‘शिक्षित’ (Educate) कर देता है ।
RP1 और अगली पीढ़ी के ऑन्कोलिटिक वायरस: नई उम्मीदें
T-VEC की सफलता के बाद, वैज्ञानिकों ने इसके प्रभाव को और अधिक शक्तिशाली बनाने के लिए ‘अगली पीढ़ी’ के वायरस विकसित किए। इसमें सबसे प्रमुख नाम RP1 (Vusolimogene Oderparepvec) का है। RP1 को ‘Replimune’ कंपनी द्वारा विकसित किया गया है और यह T-VEC की तुलना में कई गुना अधिक प्रभावी सिद्ध हो रहा है ।
RP1 और T-VEC के बीच मुख्य अंतर इसकी ‘फ्यूसोजेनिक’ (Fusogenic) क्षमता है। RP1 में ‘गिब्बन एप ल्यूकेमिया वायरस’ (GALV) से लिया गया एक विशेष प्रोटीन जोड़ा गया है। यह प्रोटीन संक्रमित कैंसर कोशिका को अपने पड़ोसी कैंसर कोशिकाओं के साथ जुड़ने (Fuse) के लिए मजबूर करता है, जिससे एक ‘मल्टी-न्यूक्लिएटेड जाइंट सेल’ या ‘सिनसिटिया’ (Syncytia) बन जाता है । यह प्रक्रिया न केवल ट्यूमर के विनाश को तेज करती है, बल्कि यह कैंसर कोशिकाओं के भीतर से अधिक एंटीजन को बाहर निकालती है, जिससे प्रतिरक्षा प्रणाली अधिक उग्र रूप से प्रतिक्रिया करती है ।
IGNYTE क्लिनिकल ट्रायल के आंकड़े बताते हैं कि RP1 ने उन रोगियों में भी 33% की प्रतिक्रिया दर दिखाई है जिन पर पहले की सभी इम्यूनोथेरेपी दवाएं विफल हो चुकी थीं । यह उन रोगियों के लिए एक जीवनदान की तरह है जिनके पास उपचार के अन्य विकल्प समाप्त हो चुके थे।
RP1 के नवीन विकास और लाभ
- बढ़ी हुई मारक क्षमता: सिनसिटिया निर्माण के कारण कैंसर कोशिकाओं का विनाश अधिक व्यापक होता है ।
- प्रणालीगत प्रतिरक्षा सक्रियण: यह ‘कोल्ड’ ट्यूमर (जहाँ प्रतिरक्षा प्रणाली सक्रिय नहीं है) को ‘हॉट’ ट्यूमर में बदल देता है ।
- उच्च उत्तरजीविता दर: IGNYTE ट्रायल में 75% रोगी एक वर्ष के बाद जीवित थे, जो उन्नत मेलेनोमा के लिए एक बड़ी उपलब्धि है ।
कार्य करने की प्रक्रिया (Mechanism of Action) का विस्तृत विश्लेषण
कैंसर के इलाज में हर्पीज वायरस का उपयोग केवल एक तरीके से काम नहीं करता, बल्कि यह एक बहु-स्तरीय (Multi-pronged) रणनीति अपनाता है। इसे समझने के लिए हमें ट्यूमर माइक्रोएन्वायरमेंट (Tumor Microenvironment) की गहराइयों में जाना होगा।
1. प्रत्यक्ष ट्यूमर विनाश (In-situ Vaccination)
जब वायरस ट्यूमर में प्रवेश करता है, तो वह कोशिका के मशीनरी पर कब्जा कर लेता है। वायरस अपनी हजारों प्रतियां बनाता है, जिससे कोशिका के भीतर दबाव बढ़ता है और अंततः वह फट जाती है। इस फटने की प्रक्रिया को ‘लाइटिक सेल डेथ’ कहा जाता है। जैसे ही कोशिका फटती है, हजारों नए वायरस कण बाहर निकलते हैं और पास की अन्य कैंसर कोशिकाओं को संक्रमित करते हैं ।
2. डेंजर सिग्नल्स का विमोचन (DAMPs and PAMPs)
कोशिका के फटने पर केवल वायरस ही बाहर नहीं निकलते, बल्कि कोशिका के भीतर के कुछ विशेष अणु भी निकलते हैं जिन्हें ‘डेंजर एसोसिएटेड मॉलिक्यूलर पैटर्न्स’ (DAMPs) कहा जाता है। इसके साथ ही वायरस के अपने घटक ‘पैथोजन एसोसिएटेड मॉलिक्यूलर पैटर्न्स’ (PAMPs) के रूप में कार्य करते हैं। ये अणु शरीर की प्रतिरक्षा प्रणाली के लिए ‘युद्ध की घोषणा’ की तरह होते हैं, जो सोई हुई प्रतिरक्षा कोशिकाओं को जगाते हैं ।
3. क्रॉस-प्रेजेंटेशन और टी-सेल सक्रियण
सबसे क्रांतिकारी हिस्सा तब होता है जब शरीर की डेंड्रिटिक कोशिकाएं इन मुक्त कैंसर एंटीजन को इकट्ठा करती हैं और उन्हें ‘टी-सेल्स’ (T-cells) को दिखाती हैं। यह ऐसा है जैसे पुलिस को अपराधी की फोटो दिखाना। अब ये टी-सेल्स पूरे शरीर में घूमते हैं और किसी भी अंग (जैसे फेफड़े या लीवर) में छिपी हुई कैंसर कोशिकाओं को पहचानकर उन्हें मारना शुरू कर देते हैं । यही कारण है कि कैंसर के इलाज में हर्पीज वायरस का उपयोग भविष्य में मेटास्टैटिक कैंसर (फैलने वाला कैंसर) के लिए सबसे प्रभावी उपचार बन सकता है ।
पारंपरिक चिकित्सा बनाम विरोथेरेपी: एक तुलनात्मक मूल्यांकन
कैंसर के उपचार के पारंपरिक तरीके जैसे कीमोथेरेपी और रेडिएशन दशकों से उपयोग किए जा रहे हैं, लेकिन उनकी अपनी सीमाएं और गंभीर दुष्प्रभाव हैं। कैंसर के इलाज में हर्पीज वायरस का उपयोग एक नई दिशा प्रदान करता है जो अधिक सटीक और कम हानिकारक है।
| तुलना का आधार | कीमोथेरेपी (Chemotherapy) | विकिरण (Radiation) | विरोथेरेपी (Herpes OVs) |
| लक्ष्य (Targeting) | शरीर की सभी तेजी से विभाजित होने वाली कोशिकाएं। | केवल वह क्षेत्र जहाँ किरणें डाली जाती हैं। | केवल कैंसर कोशिकाएं जिनमें वायरल रक्षा तंत्र की कमी है । |
| दुष्प्रभाव (Side Effects) | बाल झड़ना, अत्यधिक कमजोरी, संक्रमण का खतरा । | त्वचा का जलना, अंगों का सख्त होना, थकान। | सामान्यतः फ्लू जैसे लक्षण (बुखार, ठंड लगना) । |
| प्रतिरक्षा प्रणाली पर प्रभाव | अक्सर प्रतिरक्षा प्रणाली को कमजोर करती है। | स्थानीय स्तर पर कोशिकाओं को मारती है। | प्रतिरक्षा प्रणाली को सक्रिय और प्रशिक्षित करती है । |
| उपचार की प्रकृति | प्रणालीगत (Systemic) जहर। | स्थानीय (Local) भौतिक विनाश। | जैविक (Biological) स्मार्ट विनाश । |
| दीर्घकालिक लाभ | उपचार बंद होते ही प्रभाव कम हो सकता है। | केवल स्थानीय ट्यूमर पर प्रभाव। | ‘इम्यून मेमोरी’ के कारण लंबे समय तक सुरक्षा । |
इस तुलना से स्पष्ट है कि कैंसर के इलाज में हर्पीज वायरस का उपयोग उन रोगियों के लिए एक वरदान है जो कीमोथेरेपी की कठोरता को सहन नहीं कर सकते। विशेष रूप से बुजुर्ग रोगियों में, जहाँ अंगों की सहनशक्ति कम होती है, विरोथेरेपी एक सुरक्षित विकल्प के रूप में उभर रही है ।
2025 के नवीनतम शोध और महत्वपूर्ण चिकित्सा सफलताएं
जैसे-जैसे हम 2025 में आगे बढ़ रहे हैं, विरोथेरेपी के क्षेत्र में कुछ ऐसी सफलताएं मिली हैं जो पहले असंभव मानी जाती थीं। शोधकर्ता अब हर्पीज वायरस की सीमाओं को तोड़ने के लिए नैनोटेक्नोलॉजी और एआई (AI) का उपयोग कर रहे हैं।
एक प्रमुख सफलता ‘रक्त-मस्तिष्क बाधा’ (Blood-Brain Barrier) को पार करने में मिली है। ऐतिहासिक रूप से, मस्तिष्क के कैंसर (जैसे ग्लियोब्लास्टोमा) का इलाज करना कठिन रहा है क्योंकि अधिकांश दवाएं मस्तिष्क तक नहीं पहुँच पातीं। 2025 के नैदानिक परीक्षणों में, स्टेम सेल आधारित डिलीवरी (MSC-based delivery) का उपयोग करके हर्पीज वायरस को सफलतापूर्वक मस्तिष्क के ट्यूमर तक पहुँचाया गया है । यह न्यूरो-ऑन्कोलॉजी के क्षेत्र में एक ऐतिहासिक मोड़ है।
इसके अतिरिक्त, यूसी डेविस (UC Davis) के वैज्ञानिकों ने एक ‘जेनेटिक ट्रोजन हॉर्स’ तकनीक विकसित की है। इसमें एक हानिरहित वायरस का उपयोग करके कैंसर कोशिकाओं के भीतर एक ऐसा जीन डाला जाता है जो एक सामान्य एंटी-वायरल दवा (Ganciclovir) को एक शक्तिशाली कैंसर-नाशक एजेंट में बदल देता है। यह तकनीक विशेष रूप से कैपोसी सारकोमा जैसे वायरस से जुड़े कैंसर में 90% से अधिक प्रभावशीलता दिखा रही है ।
2025 की प्रमुख शोध दिशाएं:
- नैनोबॉडी-एन्हांस्ड ओएचएसवी: वायरस के बाहरी आवरण को नैनोबॉडी के साथ संशोधित करना ताकि वह सीधे ट्यूमर रिसेप्टर्स से जुड़ सके ।
- कॉम्बिनेशन थेरेपी: वायरस को ‘चेकपॉइंट इनहिबिटर्स’ (जैसे Pembrolizumab) के साथ मिलाकर देना, जिससे सफलता की दर दोगुनी हो गई है ।
- पर्सनलाइज्ड विरोथेरेपी: रोगी के अपने ट्यूमर के आनुवंशिक प्रोफाइल के आधार पर वायरस को कस्टमाइज करना ।
सफलता की दर और नैदानिक आंकड़े (Clinical Statistics)
कैंसर के इलाज में हर्पीज वायरस का उपयोग की प्रभावशीलता को मापने के लिए वैज्ञानिक ‘ऑब्जेक्टिव रिस्पांस रेट’ (ORR) और ‘ओवरऑल सर्वाइवल’ (OS) जैसे मानकों का उपयोग करते हैं। विभिन्न अध्ययनों के आंकड़े बताते हैं कि विरोथेरेपी ने उन क्षेत्रों में भी परिणाम दिए हैं जहाँ पारंपरिक दवाएं विफल रही थीं।
| कैंसर का प्रकार | उपचार पद्धति | प्रतिक्रिया दर (Response Rate) | जीवित रहने की दर (2 वर्ष) |
| उन्नत मेलेनोमा | RP1 + Nivolumab | 32.9% | 63.3% |
| हॉजकिन लिंफोमा | इम्यूनोथेरेपी आधारित | >60% | उच्च |
| मल्टीपल मायलोमा | Talquetamab (प्रायोगिक) | 73% | परीक्षण जारी |
| फेफड़ों का कैंसर (NSCLC) | Pembrolizumab + Virus | 20-30% | 23.2% (5 वर्ष) |
| मूत्राशय का कैंसर | OH2 वायरस थेरेपी | 20-25% | मध्यम |
ये आंकड़े स्पष्ट करते हैं कि कैंसर के इलाज में हर्पीज वायरस का उपयोग एक ‘गेम-चेंजर’ है। विशेष रूप से, ‘कंपलीट रिस्पांस’ (CR) प्राप्त करने वाले रोगियों की संख्या में वृद्धि हुई है, जिसका अर्थ है कि उनके शरीर में कैंसर का कोई भी पहचान योग्य निशान शेष नहीं बचा । जॉन हॉपकिंस विश्वविद्यालय के शोध के अनुसार, इम्यूनोथेरेपी आधारित वायरस उपचारों ने उन रोगियों के पांच साल जीवित रहने की संभावना को तीन गुना कर दिया है जो पहले केवल कुछ महीनों की उम्मीद कर रहे थे ।
भारत में विरोथेरेपी की स्थिति: उपलब्धता और चुनौतियां
भारत में कैंसर के इलाज में हर्पीज वायरस का उपयोग अभी अपने प्रारंभिक लेकिन उत्साहजनक चरण में है। भारत दुनिया के उन देशों में शामिल है जहाँ कैंसर का बोझ बहुत अधिक है, और यहाँ के डॉक्टर आधुनिक तकनीकों को अपनाने में अग्रणी रहे हैं।
उपलब्धता: वर्तमान में, T-VEC (Imlygic) भारत के कुछ चुनिंदा कैंसर विशेषज्ञ केंद्रों (जैसे टाटा मेमोरियल, अपोलो और मैक्स) में उपलब्ध है । हालांकि, इसकी उच्च लागत और विशिष्ट भंडारण आवश्यकताओं (जैसे -70°C तापमान) के कारण यह अभी तक ग्रामीण क्षेत्रों तक नहीं पहुँच पाया है।
लागत: भारत में विरोथेरेपी की लागत एक बड़ी चुनौती है। एक अनुमान के अनुसार, इस उपचार के एक पूरे चक्र की लागत ₹2,50,000 से ₹10,00,000 के बीच हो सकती है, जो उपयोग किए गए वायरस के प्रकार और खुराक की संख्या पर निर्भर करती है । हालांकि, भारत में विकसित की जा रही ‘स्वदेशी विरोथेरेपी’ और नैदानिक परीक्षणों के माध्यम से भविष्य में इसकी लागत कम होने की उम्मीद है।
क्लीनिकल ट्रायल: भारत में कई अंतरराष्ट्रीय क्लीनिकल ट्रायल (जैसे IGNYTE-3) के साइट्स मौजूद हैं। रोगी इन परीक्षणों में भाग लेकर मुफ्त या कम लागत पर इन आधुनिक उपचारों का लाभ उठा सकते हैं । ‘डेन्वैक’ (Denvax) जैसे भारतीय संस्थान भी ऑन्कोलिटिक वायरस और इम्यूनोथेरेपी के संयोजन पर गहन शोध कर रहे हैं ।
रोगी सुरक्षा और दुष्प्रभाव प्रबंधन: एक संपूर्ण गाइड
कैंसर के इलाज में हर्पीज वायरस का उपयोग करते समय सुरक्षा सबसे महत्वपूर्ण पहलू है। चूंकि यह एक ‘जीवित’ वायरस है, इसलिए इसके प्रशासन और बाद की देखभाल के लिए विशेष प्रोटोकॉल का पालन करना अनिवार्य है।
प्रशासन की प्रक्रिया (Step-by-Step Guide)
- परामर्श और पात्रता: डॉक्टर यह सुनिश्चित करते हैं कि रोगी की प्रतिरक्षा प्रणाली बहुत अधिक कमजोर न हो (जैसे HIV या सक्रिय ल्यूकेमिया के मामले में) ।
- इंजेक्शन: अल्ट्रासाउंड या प्रत्यक्ष दृष्टि का उपयोग करके वायरस को सीधे ट्यूमर में इंजेक्ट किया जाता है। सबसे बड़े ट्यूमर को प्राथमिकता दी जाती है ।
- अवलोकन: इंजेक्शन के बाद रोगी को कुछ घंटों तक अस्पताल में रखा जाता है ताकि किसी भी तत्काल एलर्जी प्रतिक्रिया की जांच की जा सके।
संभावित दुष्प्रभाव और उनका प्रबंधन
विरोथेरेपी के दुष्प्रभाव कीमोथेरेपी की तुलना में बहुत हल्के होते हैं। अधिकांश रोगियों को ‘फ्लू जैसे लक्षण’ महसूस होते हैं।
- बुखार और ठंड लगना: यह संकेत है कि शरीर की प्रतिरक्षा प्रणाली सक्रिय हो रही है। इसके लिए सामान्य पैरासिटामोल दी जाती है ।
- थकान और मतली: ये लक्षण आमतौर पर 48-72 घंटों के भीतर अपने आप ठीक हो जाते हैं ।
- इंजेक्शन स्थल की प्रतिक्रिया: सूजन या लालिमा होने पर ठंडी सिकाई की सलाह दी जाती है ।
स्वच्छता के महत्वपूर्ण नियम (Hygiene Protocol)
चूंकि वायरस संक्रमित ट्यूमर से बाहर निकल सकता है, इसलिए परिवार के अन्य सदस्यों की सुरक्षा के लिए निम्नलिखित सावधानियां जरूरी हैं:
- पट्टी का उपयोग: इंजेक्शन वाली जगह को कम से कम 7 दिनों तक वाटरप्रूफ पट्टी से ढंक कर रखें ।
- दस्ताने पहनना: यदि पट्टी बदलनी हो, तो देखभाल करने वाले को हमेशा डिस्पोजेबल दस्ताने पहनने चाहिए ।
- सुरक्षित निपटान: उपयोग की गई पट्टियों को एक प्लास्टिक बैग में सील करके कचरे में डालें ।
- सीधा संपर्क टालें: उपचार के दौरान और उसके कुछ समय बाद तक घाव या शारीरिक तरल पदार्थों के सीधे संपर्क से बचें ।
अक्सर पूछे जाने वाले प्रश्न (FAQs)
प्रश्न 1: क्या कैंसर के इलाज में हर्पीज वायरस का उपयोग करने से मुझे सामान्य हर्पीज की बीमारी हो जाएगी? उत्तर: नहीं। चिकित्सा में उपयोग किया जाने वाला वायरस आनुवंशिक रूप से संशोधित (Attenuated) होता है। इसके बीमारी फैलाने वाले जीन (जैसे ICP34.5) को हटा दिया जाता है, जिससे यह सामान्य कोशिकाओं को संक्रमित नहीं कर पाता और हर्पीज के लक्षण पैदा नहीं करता ।
प्रश्न 2: क्या यह उपचार कीमोथेरेपी से बेहतर है? उत्तर: यह ‘बेहतर’ या ‘बदतर’ का सवाल नहीं है, बल्कि ‘सटीकता’ का है। विरोथेरेपी केवल कैंसर कोशिकाओं को मारती है, जबकि कीमोथेरेपी स्वस्थ कोशिकाओं को भी नुकसान पहुँचाती है। कई मामलों में, डॉक्टर इन दोनों को साथ में देने की सलाह देते हैं ताकि सर्वोत्तम परिणाम मिल सकें ।
प्रश्न 3: किन कैंसर रोगियों को यह उपचार नहीं लेना चाहिए? उत्तर: गर्भवती महिलाएं, अंग प्रत्यारोपण कराने वाले व्यक्ति, और वे लोग जिनकी प्रतिरक्षा प्रणाली गंभीर रूप से कमजोर है (जैसे AIDS के रोगी), उन्हें इस उपचार से बचना चाहिए ।
प्रश्न 4: क्या यह इलाज भारत में बहुत महंगा है? उत्तर: हाँ, वर्तमान में यह एक महंगा उपचार है क्योंकि अधिकांश दवाएं आयात की जाती हैं। हालांकि, सरकारी अस्पतालों और क्लीनिकल ट्रायल्स के माध्यम से इसे सस्ता बनाने के प्रयास जारी हैं ।
प्रश्न 5: क्या इस इलाज के बाद बाल झड़ते हैं? उत्तर: नहीं। विरोथेरेपी का बालों के झड़ने (Alopecia) से कोई संबंध नहीं है। यह कीमोथेरेपी का एक विशिष्ट दुष्प्रभाव है जो विरोथेरेपी में नहीं देखा जाता ।
प्रश्न 6: उपचार के कितने समय बाद परिणाम दिखने लगते हैं? उत्तर: आमतौर पर, ट्यूमर के आकार में कमी दूसरी या तीसरी खुराक के बाद (लगभग 6-8 सप्ताह) दिखाई देने लगती है। हालांकि, पूर्ण प्रतिरक्षा प्रतिक्रिया बनने में 3-6 महीने का समय लग सकता है ।
प्रश्न 7: क्या यह फेफड़ों या लीवर के कैंसर के लिए भी काम करता है? उत्तर: वर्तमान में स्वीकृत दवाएं मुख्य रूप से त्वचा और लिम्फ नोड्स के लिए हैं। लेकिन 2025 के शोधों के अनुसार, लीवर और फेफड़ों के ट्यूमर के लिए भी नए वायरस विकसित किए जा रहे हैं जो क्लीनिकल ट्रायल के अंतिम चरणों में हैं ।
प्रश्न 8: क्या इलाज के दौरान संभोग करना सुरक्षित है? उत्तर: सुरक्षा के लिहाज से, उपचार के दौरान और अंतिम खुराक के 30 दिन बाद तक सुरक्षित यौन संबंध (कंडोम का उपयोग) बनाने या परहेज करने की सलाह दी जाती है ताकि वायरस के प्रसार की किसी भी संभावना को रोका जा सके ।
निष्कर्ष: भविष्य की ओर एक कदम
कैंसर के इलाज में हर्पीज वायरस का उपयोग चिकित्सा विज्ञान की उस अदम्य जिजीविषा का प्रतीक है जो मृत्यु के दूत को जीवन के दूत में बदलने की क्षमता रखती है। हम एक ऐसे भविष्य की ओर बढ़ रहे हैं जहाँ कैंसर का इलाज केवल ‘जहर’ (कीमो) या ‘जलाने’ (रेडिएशन) तक सीमित नहीं रहेगा, बल्कि यह एक सूक्ष्म लेकिन अत्यंत सटीक ‘जैविक युद्ध’ होगा। ऑन्कोलिटिक विरोथेरेपी ने यह सिद्ध कर दिया है कि हमारे शरीर के भीतर ही कैंसर को हराने की शक्ति मौजूद है, बस उसे सही ‘मार्गदर्शन’ की आवश्यकता है।
आने वाले दशक में, जैसे-जैसे एआई-संचालित प्रोटीन डिजाइन और नैनोटेक्नोलॉजी और अधिक परिष्कृत होगी, हम शायद ऐसे ‘यूनिवर्सल विरोथेरेपी’ देखेंगे जो एक ही इंजेक्शन से शरीर के किसी भी हिस्से के कैंसर को पहचानकर नष्ट कर देगी । हालांकि अभी भी लागत और व्यापक उपलब्धता जैसी चुनौतियां हमारे सामने हैं, लेकिन 2025 के आंकड़े और सफल रोगी कहानियाँ हमें विश्वास दिलाती हैं कि कैंसर के खिलाफ हमारी लड़ाई अब अंतिम और सबसे प्रभावी चरण में पहुँच चुकी है। कैंसर के इलाज में हर्पीज वायरस का उपयोग केवल एक विकल्प नहीं है, बल्कि यह उस नई सुबह की किरण है जहाँ कैंसर अब ‘असाध्य’ नहीं रहेगा।